FDA将于近日发布新增II类产品中豁免510(k)申请的品类,这一举措将有助于降低这些产品的注册门槛,并降低厂家在注册方面所需支付的费用。
FDA在综合考虑产品的特性和产品的上市历史及其他重要因素后决定,下表所列产品将在今后豁免510(k)(上市前通告)程序。
表1 豁免510(k)的II类产品
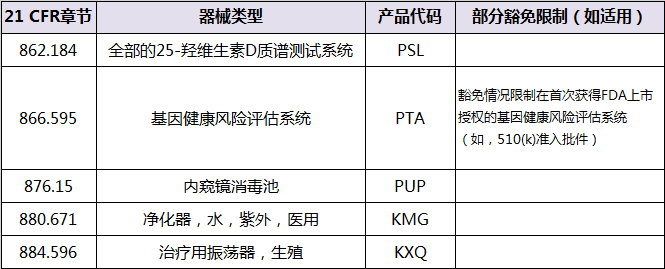
这类产品的厂家,可根据所处状态和自身具体情况来制定相应的应对方案:
1) 正在进行这类产品510(K)申请厂家应与510(K)主审评员沟通:如符合条件,则可以撤回申请或取得“本产品为豁免类产品”的通知书;如超过限定条件,则继续进行审评
2) 已取得上市通知的厂家无需进行任何操作
3) 如产品属于部分豁免类产品的非豁免部分,则要在需要进行510(K)申请时遵循现有法规和指导原则来进行申请
准备好开始了吗?
那就与我们取得联系吧